ĪĪĪĪßt╦ÄŠW11į┬21╚šėŹĪĪ╚šŪ░Ż¼║■▒▒╩Ī╦Ä▒OŠų░l▓╝┴╦ĪČĻPė┌╬ę╩Īßt»¤Ų„ąĄĮøĀIŲ¾śIĮ╗▓µÖz▓ķŪķørĄ─═©ł¾ĪĘŻ¼╣▓Öz▓ķ┴╦117╝ęßt»¤Ų„ąĄĮøĀIŲ¾śIŻ¼Ųõųą74╝ę┤µį┌å¢Ņ}Ż¼╩▄ĄĮ▓╗═¼│╠Č╚Ą─╠Ä┴PĪŻ
ĪĪĪĪųĄĄ├ūóęŌĄ─╩ŪŻ¼į┌75╝ęå¢Ņ}ßtąĄĮøĀIŲ¾śIųąŻ¼ėąČÓ▀_23╝ę╩Ū▒╗ų▒Įėę¬Ū¾═ŻśIš¹Ė─Ą─Ż¼4╝ę▒╗▀Mę╗▓Į╗“Ė·█Ö║╦▓ķ║╦īŹŻ¼Ųõ╦¹47╝ęŠ∙▒╗ž¤┴ŅŽ▐Ų┌š¹Ė─ĪŻ
ĪĪĪĪ═©ł¾ĘQŻ¼┤╦┤╬Öz▓ķ░l¼FĄ─ų„ę¬å¢Ņ}░³└©Ż║
ĪĪĪĪ1Īó│¼ĘČć·ĮøĀIßt»¤Ų„ąĄĪŻéĆäe┴Ń╩█╦ÄĄĻ╬┤╚ĪĄ├Č■ŅÉéõ░Ėæ{ūCõN╩█Č■ŅÉßt»¤Ų„ąĄĪŻ
ĪĪĪĪ2Īó╔├ūįūāĖ³įS┐╔Ż©éõ░ĖŻ®╩┬ĒŚĪŻéĆäeŲ¾śI╔├ūįĖ─ūāŲ¾śI├¹ĘQĪóé}ÄņĄžųĘŻ¼£p╔┘ĮøĀI├µĘeŻ¼╔§ų┴╚ĪŽ¹é}ÄņŻ¼«aŲĘĄ─ĮøĀI┤µā”Śl╝■ėą▓╗═¼│╠Č╚Ą─Ė─ūāĪŻ
ĪĪĪĪ3Īó┘|┴┐╣▄└Ē╚╦åT╬┤─▄▒M┬Ü▒Mž¤ĪŻ▓┐ĘųŲ¾śI┘|┴┐╣▄└Ē╚╦åT▓╗╩ņŽżßt»¤Ų„ąĄ▒OČĮ╣▄└ĒĘ©ęÄĪóęÄš┬Ż¼▓╗ųžęĢĘ©┬╔Ę©ęÄ┼Óė¢Ż╗▓┐ĘųŲ¾śI╩š╝»╔ŽŽ┬ė╬┘Y┘|▓╗═Ļš¹Ż¼▓╗─▄╠ß╣®┘|┴┐▒ŻūCģfūhĪóĘ©╚╦╩┌ÖÓ╬»═ąĢ°Īóßt»¤Ų„ąĄÖz“׳¾ĖµĢ°Ą╚ĪŻ
ĪĪĪĪ4Īó┘A▀\Śl╝■▓╗Ę¹║Žę¬Ū¾ĪŻéĆäeŲ¾śIé}Äņ╣▄└Ē╗ņüyŻ¼«aŲĘ╬┤░┤ę¬Ū¾Ęųģ^┤µĘ┼Ż¼ųŲČ©Ą─┘|┴┐╣▄└ĒųŲČ╚╬┤ėąą¦ł╠ąąŻ╗ī”ąĶꬥ═£žĪó└õ▓žßt»¤Ų„ąĄ▀Mąą╚½µ£Śl└õµ£╣▄└ĒĄ─Ż¼▓┐ĘųŲ¾śI¤o└õµ£▀\▌öĮ╗Įėå╬Īó¤oį┌═Š£žČ╚ėøõøŻ╗▓┐ĘųŲ¾śI╬┤░┤ššßt»¤Ų„ąĄšf├„Ģ°║═ś╦║ל╦╩Šę¬Ū¾▀\▌öĪó┘A┤µßt»¤Ų„ąĄŻ¼é}Äņ£žØ±Č╚ėøõø▓╗╚½ĪŻ
ĪĪĪĪ═©ł¾ę¬Ū¾Ż¼Ė„╩ąų▌╩│╦Ä▒OŠųæ¬ī”▌Āģ^ā╚ßt»¤Ų„ąĄĮøĀIŲ¾śI┤µį┌Ą─┘|┴┐╣▄└Ēå¢Ņ}ę└Ę©ę└ęÄ▀Mąą╠Ä└ĒŻ¼ī”ć└ųž▀`Ę©▀`ęÄąą×ķę¬┴ó░Ė▓ķ╠ÄĪóų▒ų┴Ą§õNßt»¤Ų„ąĄĮøĀIįS┐╔ūCĪŻ═¼Ģrī”Ų¾śIš¹Ė─┬õīŹŪķør▀MąąĖ·█ÖÖz▓ķŻ¼▓óīóŲ¾śIš¹Ė─Ūķør║═░Ė╝■▓ķ╠ÄŪķørė┌2016─Ļ12į┬2╚šŪ░╔Žł¾║■▒▒╩ĪŠųĪŻ
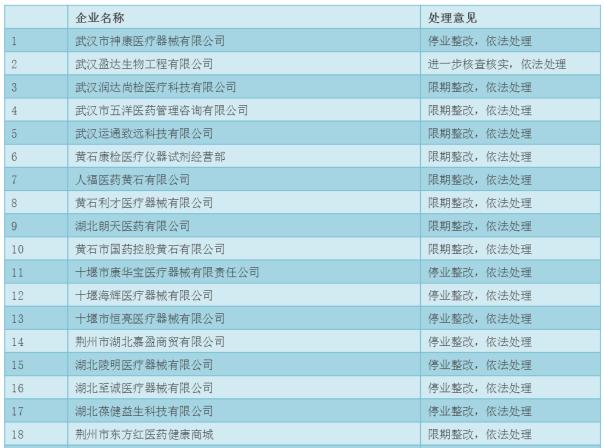
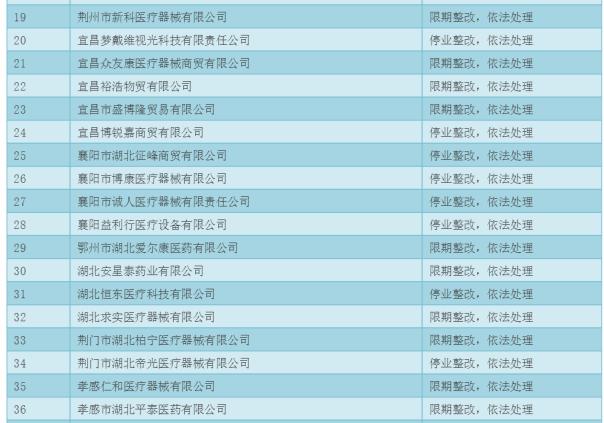
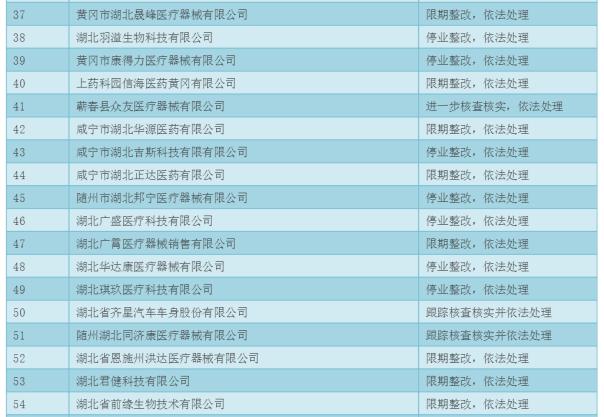
ĪĪĪĪ║■▒▒╩Īßt»¤Ų„ąĄĮøĀIŲ¾śIĮ╗▓µÖz▓ķ░l¼F┤µį┌å¢Ņ}Ą─Ų¾śI╝░╠Ä└ĒęŌęŖ▒ĒŻ║
|
